Infección
en Cirugía
|
|
|
Dr. Washington Alemán-Espinoza
|
|
Dra. Greta Mińo-León
|
Infección del Sitio Quirúrgico y
Profilaxis Antimicrobiana Preoperatoria
Antecedentes
| Publicidad |
|

|
Las infecciones relacionadas a cirugía han
plagado la humanidad a través de los ańos y los esfuerzos para controlarlos han
determinado tres épocas: la primera, desde la prehistoria hasta 1860, en la cual se
manejaba en forma empírica las heridas, la segunda de 1863 a 1940 dada por la práctica
quirúrgica aséptica y antiséptica a partir del conocimiento de la patogénesis
bacteriana de la infección y la tercera desde 1940 hasta el presente determinada por la
aparición de los antibióticos.1
En 1862, Luis Pasteur establecía los
conceptos de sepsis y asepsia, tres ańos después Joseph Lister demostraba la acción de
la antisepsia en la cirugía ortopédica con la aplicación de fenol.2,3 Este
método de antisepsia fue gradualmente aceptado por otros. La verdadera revolución de la
era de los antibióticos determinó que los procedimientos quirúrgicos fuesen cada vez
más complejos, invasivos, y en definitiva fuesen un impulso importante para el desarrollo
de la cirugía moderna. La utilización de métodos de barrera como guantes, mascarillas,
instrumental quirúrgico estéril fue convirtiéndose en rutina estándar para los
procedimientos quirúrgicos. La introducción de la profilaxis quirúrgica constituyó
otro avance de importancia, estudios tanto experimentales como clínicos demostraron una
disminución en la frecuencia de infección de herida quirúrgica. Tomó tiempo evidenciar
la efectividad de los antibióticos en la profilaxis de la infección de la herida
quirúrgica. Hubo mucha controversia en relación a la dosis, y el momento que debía
administrarse los antibióticos hasta que 2 cirujanos americanos, Burke y Polk en 1959
conjuntamente con Miles en Londres en 1967 demostraron que la profilaxis era exitosa si
niveles tisulares elevados del antibiótico adecuado se establecía antes de que ocurra la
contaminación bacteriana en el momento quirúrgico.4 Esta información fue
aplicada a pacientes sometidos a procedimientos quirúrgicos electivos, demostrando
resultados clínicos efectivos con significancia estadística.5 Los
antibióticos no eliminan por completo el peligro de infección y además nunca sustituyen
la práctica quirúrgica correcta. Desde entonces los antibióticos profilácticos han
probado ser muy útiles en intervenciones quirúrgicas donde se anticipó la
contaminación endógena.4
Los tres principios de antisepsia, asepsia
y profilaxis quirúrgica han sido los mayores avances en cirugía en las últimas
décadas, y actualmente procedimientos extremadamente complicados pueden ser realizados de
manera relativamente segura y en grandes escalas apoyados por los antibióticos los cuales
son extraordinariamente efectivos en el tratamiento de infecciones quirúrgicas. 3,8
En las infecciones quirúrgicas debe
considerarse diferentes elementos: el agente etiológico, el que se ha modificado debido
al creciente desarrollo sofisticado de tecnología de apoyo por el cual los pacientes
críticos tienen mejor sobrevida, siendo inicialmente las bacterias, y de ellas aquellas
que han desarrollado mecanismos de resistencia, y otros microorganismos como hongos, virus
y hasta protozoarios. Por otro lado los mecanismos de defensa alterados del hospedero son
otro determinante de infección y por último el ambiente, los factores locales, en el
cual se produce la infección.
Existen aspectos importantes en relación a
los antimicrobianos que el cirujano debe conocer. Por ejemplo debe de escogerse el
antibiótico de primera línea o de elección contra el microorganismo sospechado, tomando
en cuenta las bacterias más frecuentes en dicho tipo de infección, el órgano afecto y
en lo posible evaluar adecuadamente la sensibilidad antimicrobiana específica para
determinado gérmen, en especial, en infecciones severas. Por otro lado debe evaluarse los
hallazgos clínicos y los cambios hematológicos.
Si bien existen diferentes aspectos a
considerar en relación a infecciones en cirugía, a menudo el cirujano se encuentra en su
práctica habitual con dos de ellos: la profilaxis antibiótica preoperatoria y la
infección del sitio quirúrgico o más conocida como infección de herida quirúrgica, en
los cuales debe tener destreza para su manejo.
Infección de Sitio Quirúrgico (ISQ)
Aproximadamente 23 millones de pacientes
cada ańo son sometidos a intervenciones quirúrgicas en los Estados Unidos y alrededor de
900.000 pacientes presentan infección de herida quirúrgica, variando la tasa de
infección entre el 3 y 9 %, dependiendo de la institución y del procedimiento
específico realizado.2 La ISQ ocurre en 14 - 16% de todas las infecciones
nosocomiales entre pacientes ingresados y es la tercera causa más frecuente de infección
nosocomial reportada. Para reducir el número de ISQ deben definirse estrategias tales
como la misma definición estandarizada de infección, los métodos de vigilancia efectiva
con retroalimentación de la información a los cirujanos y en general al staff clínico.9,10,20
Microbiología
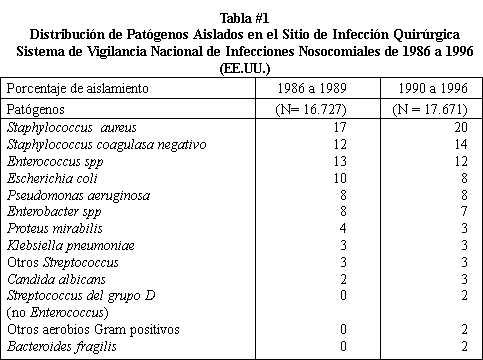
De acuerdo a los datos del Sistema Nacional
de Vigilancia de Infecciones Nosocomiales del Centro de Control de Enfermedades (CDC) la
distribución de los patógenos aislados no ha cambiado mayormente en la última década3,11
(Tabla 1). El Staphylococcus aureus y S. coagulasa negativo, Enterococcus
y Escherichia coli persisten como los microorganismos más frecuentes,
observándose un incremento de los patógenos resistentes como Staphylococcus aureus
resistente a meticilina (SARM) o por Candida albicans. De 1991 a 1995 la incidencia
de infecciones fúngicas aumento del 0,1 a 0,3 por 1000 egresos.11 El aumento
de la incidencia de gérmenes resistentes y Candida se debe a un mayor número de
pacientes gravemente enfermos, inmunocom-prometidos y el impacto del uso de
antimicrobianos de amplio espectro. De una revisión en Karachi, Pakistán en Septiembre
1999, de 120 muestras de varios tipos de sitios quirúrgicos se encontraron 153 bacterias
siendo los más comunes Staphylococcus aureus (50.32%) 50% de ellos
meticilinoresistentes, seguido por Pseudomonas aeruginosa (16.3%), Escherichia
coli (14.37%) estos dos últimos resistentes a gentamicina, Klebsiella pneumoniae
(11.76%).14 Otros estudios como el realizado en México por la Dra Volkow entre
Enero 1993 y Junio 1994 se encontró una tasa de infección quirúrgica de 9.3 de un total
de 313 infecciones de sitio quirúrgico en 3372 cirugías, ligeramente un poco más alta
que en hospitales generales.15
|
|
|
 |
Es importante conocer los diferentes
microorganismos tanto de la flora exógena como endógena que podrían provocar
complicaciones infecciosas, lo cual también es útil para una correcta elección
empírica de los antibióticos.
La Flora Exógena se compone de
aerobios, existiendo cientos de especies bacterianas, entre los que más se destacan el Staphylococcus
aureus, los agentes coliformes en especial la E. coli, Staphylococcus epidermidis,
Pseudomonas, Citrobacter, enterobacterias y Clostridium.
La Flora Endógena es responsable de
un gran número de infecciones quirúrgicas. Los patógenos primarios son aquellos que se
encuentran en concentraciones reducidas en la flora total que pueden invadir los tejidos;
elaboran toxinas, enzimas, y otras sustancias que promueven su capacidad agresora. Los
patógenos secundarios también se encuentran en la flora habitual; son poco virulentos y
en general no producen compuestos que podrían favorecer la diseminación; en cambio
poseen resistencia intrínseca a diferentes antimicrobianos o la desarrollan con rapidez
merced a diversos mecanismos extracromosómicos, por lo tanto, cuando los patógenos
primarios son destruidos, los secundarios refractarios y/o resistentes podrían persistir
si el sistema de defensa del hospedero se deteriora y hay un aumento del inóculo
bacteriano, cruzando las barreras de protección y tornándose invasores.
La Flora Cutánea, es importante ya
que la piel no es estéril, la colonización bacteriana comienza al nacer y a las 2
semanas se observa flora normal, es más frecuente en áreas húmedas como los pliegues
cutáneos. Los bacterias más comunes son los aerobios Staphylococcus epidermidis,
los micrococos, los anaerobios Propionibacterium acnes y los difteroides. En
ciertas circunstancias se agregan otros como Escherichia coli, Staphylococcus aureus,
Pseudomonas aeruginosa, Candida albicans.
La Flora Gastrointestinal es
anaeróbica y aeróbica. Los anaerobios incluyen Bacteroides, Peptoestreptococcus,
bifidobacterias, fusobacterias, clostridium y eubacterias. Los aerobios abarcan
coliformes, Streptococcus, lactobacillus y hongos. La flora no es igual en todo el
tubo digestivo; en las vísceras huecas se distinguen dos tipos de microorganismos: los
orales y los fecales. En los sujetos sanos, los órganos sólidos albergan poca o ninguna
bacteria.
La composición de la flora endógena en
los distintos segmentos gastrointestinales depende de mecanismos locales de control. La
gran mayoría no es patógena, está integrada por saprófitos y simbiontes útiles para
el hombre. Aunque su concentración es considerable, estos microorganismos no invaden los
tejidos ni generan productos nocivos, no exhiben resistencia compleja y los antibióticos
los destruyen con facilidad, permitiendo así que los patógenos proliferen4.
Fisiopatología de la Infección del
Sitio Quirúrgico
La infección de una herida quirúrgica
depende de factores relacionados con el paciente, sitio quirúrgico y microbiología.1,2,3
La contaminación con patógenos es el precursor de la infección del sitio quirúrgico.
Al efectuar la incisión quirúrgica, el
tejido estéril queda expuesto a un ambiente no estéril. Aunque las técnicas de asepsia
sean rigurosas, solo reducen el inóculo bacteriano, no lo eliminan4,5 aún en
quirófanos con flujo laminar las bacterias pueden ser aisladas de la superficie de la
herida quirúrgica; en gran parte es debido a que casi el 20% de las bacterias de la piel
se alojan en las glándulas sebáceas y folículos pilosos donde no pueden ser eliminados
por los antisépticos.2 Es virtualmente imposible seńalar el origen y la
frecuencia de la contaminación. La inoculación directa de la flora endógena del
paciente en el momento quirúrgico ha sido seńalada como la principal vía; aunque
también se sugiere la vía exógena, ya que estudios epidemiológicos han determinado que
los microorganismos que se encuentran suspendidos en el ambiente quirúrgico han sido
implicados también en infecciones postquirúrgicas. Mas controversial es la siembra
hematógena de la herida quirúrgica. El riesgo de infección del sitio quirúrgico puede
ser conceptualizado de acuerdo a la siguiente relación:
Dosis de contaminación bacteriana x
virulencia = Riesgo de ISQ
Resistencia del hospedero
Cuantitativamente se ha demostrado que si
un sitio quirúrgico es contaminado con >105 microorganismos por gramo de
tejido, el riesgo de ISQ es elevado11, sin embargo el inóculo bacteriano puede
ser menor en presencia de material extrańo.
Numerosas bacterias han sido implicadas
como patógenos de heridas, y varias especies de acuerdo a los diferentes procedimientos.
Existen poblaciones de pacientes como los diabéticos y los pacientes sometidos a
hemodiálisis que se encuentran colonizados en más del 50% por Staphyloccocus aureus.2
Los microorganismos pueden producir toxinas
y otras sustancias que incrementen su habilidad para invadir, producir dańo o sobrevivir
en los tejidos del hospedero. Por ejemplo los bacilos gramnegativos producen endotoxinas
lo cual estimula la producción de citoquinas y estas pueden disparar la respuesta
inflamatoria que algunas veces llevan a falla multiorgánica sistémica. Otros grupos de
patógenos poseen potentes exotoxinas que alteran la membrana celular y su metabolismo,
este es el caso de algunos Clostridium y Streptococcus. Una variedad de
microorganismos que incluye los cocos grampositivos produce un glicocálix y un
componente asociado llamado "slime" ó "lama" lo cual
altera la fagocitosis e impide la penetración de los antimicrobianos. Aunque estos y
otros factores de virulencia están bien definidos, el mecanismo de desarrollo de
infección del sitio quirúrgico no ha sido completamente determinado.
Para la mayoría de ISQ, la fuente de
patógeno es la flora endógena de la piel del paciente, membranas, mucosas o vísceras
huecas sin embargo existe patógenos especiales en cada fijo de intervención quirúrgica.
Tabla 2.
Identificación de Factores de Riesgo
Como se ha mencionado la infección de
herida quirúrgica es una compleja relación entre el inóculo bacteriano durante el
procedimiento quirúrgico y la resistencia local y sistémica del hospedero a la
infección.
El aumento de la virulencia de las
bacterias contaminantes puede aumentar la probabilidad de infección, así mismo existe
factores tales como la hospitalización prolongada, excesivo uso de antimicrobianos de
amplio espectro que lleven a una colonización con microorganismos nosocomiales y/o
resistentes.
La afectación de los mecanismos de
resistencia sistémicos del hospedero como son enfermedades concomitantes, nutrición,
infecciones distantes constituyen factores de riesgo. Existen factores locales como la
presencia de hematomas, cuerpos extrańos, isquemia, tejido necrótico,5,12 en
la tabla 3 se enumeran los principales factores de riesgo relacionados al paciente y a la
características del procedimiento quirúrgico que pueda influir en la infección de la
herida quirúrgica.12
El CDC de Atlanta, inició en 1970 el
Estudio Nacional de Infecciones Nosocomiales (NNIS) y fue elaborando diferentes sistemas
de calificación, como el Estudio de Eficiencia de Control de Infecciones Nosocomiales
(SENIC-siglas en inglés-) hasta desarrollar el Sistema de riesgo del NNIS, el cual
recolecta datos en forma prospectiva, considerando el rango del índice entre 0 a 3 y
definido por 3 variables:
a) El estado físico preoperatorio (ASA 3 o
más -Sociedad Americana de Anestesiología: ASA)
b) Duración de la cirugía mayor a T
horas, donde T es aproximadamente el 75 % de la duración de la cirugía programada. Se
calcula aproximadamente dos horas.
c) Contaminación de la herida (Contaminada
o sucia) 5,11
Clasificación de Heridas Quirúrgicas
1. Limpia ( tipo I ) Son
aquellas donde la incisión atraviesa una piel sana, sin afectar las mucosas
respiratorias, digestivas, genitourinaria, ni la cavidad orofaríngea.
2. Limpias-Contaminadas. ( tipo II )
Son aquellas en que se abordan vísceras huecas que poseen flora bacteriana endógena,
así como traumatismos; en donde los microorganismos en la herida podría superar el
umbral de 106 por gramo de tejido a partir del cual el riesgo de infección se
acrecienta.4 Por lo tanto, la contaminación puede ser suficiente para aumentar
el peligro de complicaciones sépticas, pero no tanto como para causar supuración
inevitable.
3. Contaminadas ( tipo III)
Son heridas traumáticas o quirúrgicas en la cual ha habido una transgresión mayor de la
técnica, gran contaminación a partir del tubo digestivo o ingreso en las vías
genitourinarias o biliares en presencia de orina o bilis infectadas respecti-vamente. Esto
incluye incisiones que encuentran una inflamación aguda no purulenta.
4. Sucias ( tipo IV )
Incluyen heridas traumáticas sucias o con tratamiento retardado, contaminación fecal,
cuerpos extrańos, una víscera desvitalizada o líquido purulento visible de cualquier
origen.
La identificación de ISQ conlleva una
serie de interpretaciones clínicas y de laboratorio y es imprescindible que los programas
de vigilancia standaricen los criterios para evitar sub o sobrediagnósticos.
Criterios para Definir Infección de
Sitio Quirúrgico
ISQ Incisional Superficial
La infección ocurre dentro de 30 días
después de la operación y la infección involucra solamente piel o tejido subcutáneo de
la incisión y por lo menos uno de lo siguiente:
1. Drenaje purulento, con o sin
confirmación de laboratorio, de la incisión superficial.
2. Microorganismos aislados de un cultivo
de líquido o tejido obtenido asépticamente de la incisión superficial.
3. Por lo menos uno de los siguientes
signos o síntomas de infección: dolor o hipersensibilidad, edema localizado,
enrojecimiento o calor y la incisión superficial es deliberadamente abierta por el
cirujano, al menos que la incisión sea cultivo negativo.
4. Diagnóstico de ISQ incisional
superficial por el
cirujano o médico tratante.
No reporte las siguientes condiciones como
ISQ:
1. Absceso en formación (inflamación
mínima y
descarga confinada a los puntos de
penetración de sutura)
2. Infección de episiotomía o sitio de
circuncisión del recién nacido.
3. Herida infectada de quemado.
4. ISQ incisional que se extienda en las
capas musculares y fasciales (ver ISQ incisional profunda)
Nota: Deben usarse criterios
específicos para identificar sitios infectados de episiotomía y circuncisión y heridas
de quemados.
ISQ incisional profunda
La infección ocurre dentro de 30 días
después de la operación si ningún implante es dejado en el lugar o dentro de 1 ańo si
el implante está en el lugar y la infección parece estar relacionada a la operación y
la infección involucra a tejidos blandos profundos (ej: capas musculares y fasciales) de
la incisión y por lo menos uno de lo siguiente:
1. Drenaje purulento de la incisión
profunda pero no del componente espacio /órgano del sitio quirúrgico.
2. Drenaje espontáneo se abre o es abierto
en forma deliberada por un cirujano cuando el paciente tiene por lo menos uno de los
siguientes signos o síntomas: fiebre (>38şC), dolor localizado o hipersensibilidad a
menos que el sitio sea negativo para cultivo.
3. Un absceso u otra evidencia de
infección involucrando la incisión profunda se encuentra en el examen directo, durante
la reoperación, o por examen radiológico o histopatológico.
4. El diagnóstico de una ISQ incisional
profunda por un cirujano o un médico tratante.
Notas:
1. Reporte la infección que involucre
tanto los sitios de incisión superficial y profunda como ISQ incisional profunda,
2. Reporte un ISQ de espacio/órgano que
drene a través de la incisión como una ISQ incisional profunda.
ISQ Espacio /Órgano
La infección ocurre dentro de los 30 días
después de la operación si ningún implante es dejado en el lugar o dentro de un ańo si
el implante está en el lugar y la infección parece estar relacionado a la operación, y,
La infección involucra cualquier parte de
la anatomía (ejemplo: órganos y espacios), otros que la incisión, el cual fue abierto o
manipulado durante una operación y por lo menos uno de lo siguiente:
1. Drenaje purulento de un dren que es
colocado a través de una herida en el órgano/espacio.
2. Microorganismos aislados de un cultivo
de líquido o tejido obtenido asépticamente en el órgano/espacio.
3. Un absceso u otra evidencia de
infección involucrando el espacio/órgano que es encontrado en el examen directo, durante
la reoperación, o por examen radiológico o histopatológico.
4. Diagnóstico de una ISQ de
órgano/espacio por un cirujano o médico tratante.
Recomendaciones para la Prevención de
ISQ
Las recomendaciones de CDC y del Consenso
del Hospital Infection Control Practices Advisory Committee (HICPAC) fueron dadas en 1999.
Cada recomendación es categorizada sobre la base de datos existente científicamente,
racionalidad teórica y aplicabilidad.11
Clasificación
Categoría IA Fuertemente
recomendada para su
implementación basada en estudios
clínicos bien diseńados, experimentales, o epidemiológicos.
Categoría IB. Fuertemente
recomendada para su
implementación y basada en algunos
estudios clínicos, experimentales o epidemiológicos y por fuerte evidencia racional
teórica.
Categoría II Sugerida para su
implementación y
basada por estudios clínicos o
epidemiológicos o evidencia racional teórica.
No recomendadas. En controversia;
Prácticas en las cuales hay insuficiente evidencia o
no hay consenso de que exista eficacia.
Recomendaciones
1. Preoperatorio
A) Preparación del paciente
1. Si es posible, identificar y tratar
todas las infecciones remotas al sitio quirúrgico
antes de la cirugía electiva y postponer la cirugía hasta que la infección se haya
resuelto. Categoría IA
2. No remover cabello preoperatoriamente al
menos que éste se encuentre a nivel de la incisión o
interfiera con la misma. Categoría IA
3. Si el cabello es removido, hacerlo
inmediatamente
antes de la intervención,
preferiblemente con máquina eléctrica. Categoría IA
4. Controlar adecuadamente los niveles de
glucosa sanguínea en todos los pacientes diabéticos y
particularmente evitar la hiperglicemia perioperatoriamente. Categoría IB
5. Estimular el no fumar. Al mínimo,
instruya a los
pacientes para abstenerse de fumar
cigarros, cigarrillos, pipas u otra forma de consumo de tabaco, por lo menos 30 días
antes de la operación electiva. Categoría IB
6. No retirar productos sanguíneos
necesarios de pacientes quirúrgicos como medida para
prevenir ISQ. Categoría IB
7. Bańo con un jabón antiséptico por lo
menos la noche previa al día de la intervención.
Categoría IB
8. Lave y limpie alrededor del sitio de la
incisión para remover contaminación gruesa antes de
hacer preparación de piel con antiséptico. Categoría IB
9. Use un antiséptico apropiado para
preparación de piel. Categoría IB
10. Aplicar antiséptico preoperatoriamente
en forma circular moviendo hacia la periferia, al
preparar la piel. El área preparada debe ser suficientemente grande para extender la
incisión o crear nuevas incisiones o sitios de drenaje, si es necesario. Categoría II
11. Mantenga la estancia hospitalaria
preoperatoria tan corta como sea posible. Evite
estancia hospitalaria prolongada. Categoría II.
12. No hay recomendación para retirar o
descontinuar uso de esteroides sistémicos (cuando sea
médicamente permisible) antes de operación electiva. En controversia.
13. No existe recomendación para aumentar
el apoyo nutricional para pacientes quirúrgicos
aisladamente como un medio para prevenir ISQ. En controversia
14. No existe recomendación para aplicar
Mupirocina preoperatoriamente a fosas nasales para
prevenir ISQ. En controversia
15. No existe recomendación para proveer
medidas que aumenten la oxigenación del espacio de la
herida para prevenir ISQ. En controversia
B. Antisepsia de manos y antebrazos para
miembros del equipo quirúrgico
1. Mantenga las uńas cortas. Categoría
IB.
2. Haga un cepillado quirúrgico
preoperatorio por
lo menos 2 a 5 minutos usando un
antiséptico apropiado. Cepille las manos y los antebrazos hasta los codos. Categoría
IB.
3. Luego del cepillado quirúrgico,
enjuagar con abundante agua dejando que el agua corra
desde las manos hacia los codos, secar con toalla y colocarse vestimenta y guantes
quirúrgicos. Categoría IB.
4. Limpiar exhaustivamente cada uńa previa
a realizar el primer lavado quirúrgico del día. Categoría
II.
5. No utilizar joyas en manos y antebrazos.
Categoría II.
6. No se recomienda uso de esmalte de
uńas.
En controversia.
C. Manejo de Personal Infectado o
Colonizado.
Educar y motivar al personal del área
quirúrgica que tengan enfermedades transmisibles a
reportarlas a su supervisor. Categoría IB.
Desarrollar políticas bien definidas
relacionadas a
los cuidados del paciente y
responsabilidad cuando el personal tiene enfermedades potencialmente transmisibles. Categoría
IB
Realizar cultivos apropiados en personal
que tenga lesiones supurativas de piel y excluir de las
labores hasta que el personal haya recibido un tratamiento adecuado y la infección este
resuelta. Categoría IB.
No separar al personal que esté colonizado
con organismos tales como Staphylococcus aureus
(fosas nasales, u otro sitio del cuerpo) o Streptococcus del grupo A, a menos que
el personal haya sido relacionado epidemiológicamente con diseminación del
microorganismo en el sitio de trabajo. Categoría IB
D. Profilaxis Antimicrobiana.
Administrar un agente antimicrobiano
únicamente cuando esté indicado, y su selección
esté basada sobre su eficacia contra los agentes más comunes causantes de ISQ. Categoría
IA
Administrar el antibiótico por vía
endovenosa, obteniendo concentraciones bactericidas en
el suero y el tejido al mismo tiempo que se realice la incisión quirúrgica manteniendo
niveles séricos adecuados mientras dure el evento quirúrgico. Categoría IB
Antes de cirugía electiva de colon agregar
preparación mecánica con el uso de enemas y agentes catárticos; y
la administración de antimicrobianos no absorbibles dividido en varias dosis el día
previo a la cirugía. Categoría IA
En cesárea de alto riesgo, la
administración de
antimicrobianos será luego de
clampear el cordón umbilical. Categoría IA
No
usar vancomicina rutinariamente como
profilaxis. Categoría
IB
2. Intraoperatorio
A . Ventilación
Mantener ventilación con presión positiva
en el quirófano con respecto a los corredores y áreas
adyacentes. Categoría IB
Mantener un mínimo de 15 cambios de aire
por hora, de los cuales por lo menos 3 deberían de ser
aire fresco. Categoría IB
Utilización de filtros de aire apropiados
de acuerdo a las normas establecidas. Categoría IB
Colocación de los sistemas de ventilación
en el tumbado y la salida, cercana al piso.
Categoría IB
No utilizar Radiación UV en quirófano
para prevenir ISQ. Categoría IB
Mantener cerradas las puertas de
quirófanos, a excepción de las necesarias para el
pasaje de equipos, personal y el paciente. Categoría IB
Considerar la realización de Implantes
ortopédicos en quirófanos con aire ultrafiltrado. Categoría
II
B. Limpieza y Desinfección de las
Superficies del Quirófano.
Las manchas de sangre u otros líquidos
corporales, deben de limpiarse con desinfectantes
aprobados por organizaciones protectoras del medio ambiente, antes de cada cirugía. Categoría
IB
No realizar limpiezas especiales o cierre
de quirófanos después de cirugías contaminadas o
sucias. Categoría IB
No utilizar alfombras a la entrada de los
quirófanos.
Categoría IB
Limpiar con aspiración húmeda el piso del
quirófano luego de la última operación del día o de la
noche. Categoría II
No se recomienda la desinfección de las
superficies del medio entre procedimientos
quirúrgicos, en ausencia de contaminación visible. En controversia
C. Muestra Microbiológica
No se recomienda tomar muestras ambientales
del quirófano de manera rutinaria. La realización de
este procedimiento de las superficies o del aire forma parte sólo de alguna
investigación epidemiológica. Categoría IB
D. Esterilización del Instrumental
Quirúrgico
La esterilización de todo el instrumental
quirúrgico es acorde a las guías publicadas. Categoría
IB
Se puede realizar esterilización rápida
solamente para instrumental que se requiera su
utilización inmediata, por ejemplo: algún instrumento que se cayó accidentalmente y que
se requiera su uso inmediato. Categoría IB
E. Vestimenta Quirúrgica
Utilizar mascarilla que cubra completamente
la nariz y boca al ingresar al quirófano previo al inicio del acto quirúrgico ó si el
instrumental estéril está expuesto y usar la misma durante todo el acto quirúrgico. Categoría
IB.
Utilizar gorro que cubra todo el cabello.
No utilizar protectores de calzado para
prevenir
ISQ. Categoría IB. En controversia.
Uso de guantes estériles, colocárselo
luego de la bata estéril. Categoría IB
Uso de batas quirúrgicas que sean
impermeables
Categoría IB
Cambio de vestimenta que se contamine con
sangre u otro material potencialmente infeccioso. Categoría
IB.
F. Asepsia y Técnica Quirúrgica.
Utilización de estrictas medidas de
asepsia para procedimientos de colocación de catéteres intravasculares. Categoría
IA.
Utilización de equipos y soluciones
estériles.
Categoría II
Utilice técnica quirúrgica adecuada,
minimice tejido desvitalizado y cuerpos extrańos
realizar hemostasia efectiva y elimine espacio muerto en el sitio quirúrgico. Categoría
IB
Usar sutura de piel primaria retardada o
dejar herida abierta para cerrar por segunda intención
ante sospecha de sitio quirúrgico contaminado. Categoría IB
Utilizar drenes con sistemas cerrados
colocados en un sitio distante a la herida quirúrgica
y retirarlo lo más pronto posible. Categoría IB
3. Cuidado de Herida Post-Operatoria
Utilización de gasa estéril sobre la
herida quirúrgica
por 24-48hs que ha sido suturada
primariamente. Categoría IB
Lavado de manos previo y posterior a la
manipulación de la herida quirúrgica. Categoría
IB
Cuando se requiera cambiar la gasa sobre la
herida quirúrgica usar técnica estéril. Categoría
II
Educar al paciente y familiares sobre
cuidados
propios de la herida, síntomas de ISQ y la
necesidad de reportar tales síntomas. Categoría II
No hay una recomendación para mantener
cubierta una incisión cerrada primariamente más de 48 hs, ni
el tiempo adecuado para bańarse con una herida no cubierta. Tema no resuelto.
Profilaxis Antimicrobiana
Preoperatoria
(PAP)
La profilaxis antimicrobiana es la
administración de un agente antimicrobiano dado en el momento del inicio del evento
quirúrgico. El antimicrobiano no esteriliza los tejidos pero ayuda a disminuir la carga
bacteriana que se produce por la contaminación intraoperatoria. No previene la infección
del sitio quirúrgico causada por la contaminación postoperatoria.11 La
infusión intravenosa es el modo más frecuente utilizado y esencialmente todas las
indicaciones de profilaxis antimicrobiana pertenecen a cirugías electivas en las cuales
las incisiones quirúrgicas son cerradas en el quirófano.
En la actualidad el término de Profilaxis
Antimicrobiana Preoperatoria (PAP) es el más adecuado y está claramente demostrado el
beneficio que se produce al disminuir la incidencia de infecciones postoperatorias en
cirugías donde el riesgo de infección es alto y en cirugías donde el riesgo es bajo
pero las consecuencias de infección son significativas. 1,2,3,4,6,7,8
Elección del Régimen de PAP
Adecuado
Cuatro son los principios básicos para
maximizar los beneficios de la profilaxis:
El antimicrobiano elegido tiene que ser
útil en la prevención de infección de herida quirúrgica evidenciada a través de
trabajos clínicos.
El agente utilizado tiene que ser
económico, seguro y bactericida con un espectro que abarque los probables microorganismos
responsables.
Que la dosis inicial del antimicrobiano
alcance concentraciones bactericidas en el suero y tejidos y esté relacionada con el
momento de la incisión quirúrgica
Los niveles terapéuticos se mantengan en
el suero y tejidos durante todo el acto quirúrgico e incluso pocas horas después que la
incisión ha sido cerrada en el quirófano.
La infección de herida quirúrgica
conlleva a la administración de una variedad de antimicrobianos con el consecuente
incremento de costos y una prolongación de la estancia hospitalaria favoreciendo la
emergencia de resistencia antimicrobiana. Es necesario conocer las características
farmacocinéticas de las drogas elegidas para la PAP.6
Existen varios reportes en donde se discute
los procedimientos quirúrgicos específicos en los cuales la PAP es beneficiosa, el
agente óptimo, el momento adecuado y la duración de la administración de estos agentes.
Está ampliamente aceptado el beneficio que
la PAP otorga a los procedimientos quirúrgicos del tubo digestivo, con la consecuente
exposición de la herida quirúrgica con la flora intestinal endógena. La única
excepción es la cirugía electiva del estómago por enfermedad ulceropéptica; situación
en la cual el medio ácido lleva a una muy baja densidad bacteriana endógena y el riesgo
de infección de herida quirúrgica es bajo.8,9 La PAP está recomendada para
procedimientos gastrointestinales de alto riesgo que incluyen neoplasias, úlcera
gástrica, sangrado, obstrucción (incluye estenosis pilórica) y perforación, de la
misma manera comprende pacientes que tengan antecedentes de ingesta crónica de drogas que
alteren el pH gástrico ( anti H2 o inhibidores de la bomba de protones).9 La
profilaxis también es recomendada en pacientes con obesidad mórbida. Se ha encontrado
que con esta patología, la diabetes mellitus y la presencia prolongada de un dren
quirúrgico aumentan el riesgo de infección.15 La vía biliar normalmente es
estéril, existe una baja tasa de colonización en cirugías electivas de litiasis en
pacientes jóvenes; la PAP está recomendada en pacientes con alto riesgo como ser: edad
> 60 ańos, obstrucción del conducto común, colecistitis reciente, y cirugías
recientes de vía biliar. 9
En procedimientos electivos de colon, la
frecuencia de infección es mayor en ausencia de PAP, en todos los demás procedimientos
la administración parenteral es la indicación sugerida, sin embargo en los
procedimientos del colon la administración oral y/o parenteral puede ser usada. Existen
múltiples estudios que han demostrado la eficacia de cualquiera de las dos vías, pero el
beneficio de las dos combinadas no está firmemente establecido. El procedimiento más
utilizado en los EE.UU., es la administración oral de antimicrobianos junto con limpieza
mecánica del intestino la noche previa a la cirugía y la administración parenteral de
antimicrobianos previa a la incisión quirúrgica.9
Otros procedimientos que son asociados a
una alta frecuencia de infección son los procedimientos vasculares en las extremidades
inferiores, histerectomías y cesáreas; y otros tipos de intervenciones quirúrgicas que
por su consecuencia devastadora en caso de producirse algún evento infeccioso son las
reemplazos protésicos articulares o vasculares, y los procedimientos cardíacos.
En los procedimientos urológicos y
ginecológicos que involucren el tracto gastrointestinal debe de administrarse PAP como en
cirugías generales, igualmente los histerectomías por vía vaginal tienen suficiente
argumento para la utilización de PAP. La utilización de esquemas de PAP cortos (<24H)
se ha observado que es eficaz.13 Existen reportes en donde el grosor de tejido
subcutáneo parece ser el único factor de riesgo significativo asociado con infección de
herida abdominal después de cesárea.16
Los procedimientos urológicos que no
involucran el tubo digestivo y la orina es estéril son considerados como cirugías
limpias y no requieren PAP, si la orina está infectada es preferible esterilizarla previa
a la cirugía y si no es posible la PAP debe de tener cobertura para los probables agentes
etiológicos y continuar el tratamiento de la infección urinaria.
La PAP en pacientes con lesiones
ortopédicas está bien establecida. Para fracturas cerradas manejadas con fijación
interna, la PAP disminuye aproximadamente al 2% comparada con el 6% de pacientes que no
recibieron PAP.4 En fracturas abiertas la severidad de la fractura así como el
compromiso de partes blandas son los factores más importantes a relacionar con procesos
infecciosos. De acuerdo a la clasificación de Gustilo las fracturas grado I, II, IIIA la
administración de cefalosporina de primera generación (cefazolina) en períodos cortos
(no > 24 horas) es lo indicado, para fracturas tipo IIIB y IIIC la posibilidad de
infección es mayor variando de 9 al 80% 4 por lo que la indicación
probablemente es la de tratamiento de infección de piel y partes blandas21
igualmente los procedimientos efectuados en salas de urgencia se relacionan a una mayor
tasa de ISQ así tenemos que en un estudio efectuado en un Hospital Universitario de
Holanda durante 3 meses se evaluaron 259 procedimientos quirúrgicos en relación al
desarrollo de infección del sitio quirúrgico: 17 se infectaron ( tasa promedio de 6.6%),
en sitios sucios la tasa aumentó al 30%, siendo de mayor riesgo los procedimientos de
emergencia y la duración de la intervención quirúrgica mayor de 60 minutos17.
También se han tratado de estudiar posibles factores de riesgo para el desarrollo de ISQ
en cirugía ortopédica con implantes protésicos, entre ellos: edad, género, método de
remoción de vello, duración de la IQ, cirujano, enfermedad subyacente, y ser portador de
S. aureus.18
La selección de un agente antimicrobiano
puede ser confusa, existen múltiples trabajos con diferentes agentes antiinfecciosos. En
términos generales el uso de cefazolina para cirugías que no involucren el íleo distal,
colon o apéndice es el antimicrobiano preferido tanto por su cobertura antimicrobiana
como por sus características farmacodinámicas y farmacocinéticas.2,8,9 Para
cirugías del tubo digestivo desde el íleo distal hasta el colon la cobertura de
antimicrobianos que tengan actividad contra anaerobios obligados del colon, incluyendo
Bacteroides fragilis es la regla, clindamicina, metronidazol combinado con
aminoglucósidos, es una de las combinaciones más recomendadas, el aztreonam junto con
clindamicina es una combinación en la cual se obvia la toxicidad de los aminoglucósidos,
la combinación de aztreonam con metronidazol no tiene cobertura adecuada para cocos gram
positivos y puede aumentar la frecuencia de infecciones por Staphyloccocus aureus,
en caso de utilizar esta combinación debe de agregarse un antimicrobiano con cobertura
para cocos gram positivos.
|
|
|
 |
Pacientes de alto riesgo con injurias de
colon u otra víscera hueca en trauma abdominal penetrante no son de mayor riesgo para
infección de sitio quirúrgico o no quirúrgico cuando son tratadas con un curso de 24
horas de antibioticoterapia.19 La utilización de antimicrobianos con cobertura
para Enteroccocus es controversial; existen múltiples trabajos en donde no se ha
demostrado que disminuya la incidencia de infecciones del sitio quirúrgico cuando se
compara con regímenes que no tienen dicha cobertura. Regímenes que tengan actividad
contra Enteroccocus como es ampicilina, amoxicilina, o Vancomicina combinada con
gentamicina son recomendados como profilaxis de endocarditis en pacientes con factores de
riesgo cardiológicos cuando se van a efectuar manipulaciones o procedimientos en el
tracto gastrointestinal o genitourinario. 2,3,9,12
La Vancomicina es la droga alternativa para
pacientes alérgicos a las cefalosporinas y en sitios donde la prevalencia de Staphyloccocus
aureus meticilinoresistente sea alta, y dado que la Vancomicina no tiene actividad contra
bacilos gramnegativos, en circunstancias donde se necesite ampliar la cobertura debe
agregarse otro antimicrobiano que puede ser la misma cefazolina.9
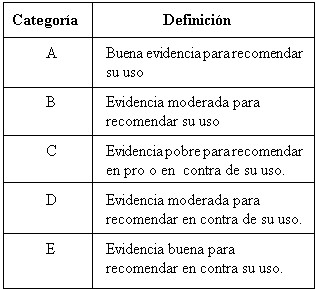
Definiciones de la Solidez de las
Recomendaciones y la Calidad de la Evidencia de las mismas 5,9,22
1. Categorías que reflejan la Solidez de
las Recomendaciones:
Recomendaciones de PAP en Cirugía
Procedimientos
La administración de PAP debe ser
administrada en los siguientes procedimientos:9,22
a) Cirugía del tracto digestivo con
apertura de mucosas (A1)
-
Esófago. (A1)
-
Estómago en pacientes de alto riesgo;
neoplasias, úlcera gástrica sangrante u obstrucción, obesidad mórbida o en pacientes
con supresión de la acidez gástrica yatrogénica o natural. (AI)
-
Cirugía del intestino delgado o vía
biliar en pacientes de alto riesgo como son síntomas recientes de inflamación
(colecistitis), obstrucción de la vía biliar común, ictericia o cirugía biliar previa.
(AI)
-
Cirugía de colon. (AI)
-
Cirugía de apéndice siempre que no
exista signos de perforación en cuyo caso debe de administrarse tratamiento y no
profilaxis.(AI)
-
Cirugía de cabeza y cuello con abordaje
por la orofaringe. (AI)
-
Cirugías vasculares tanto abdominal como
en los miembros inferiores. (AI).
-
Craniotomía. (AI)
-
Procedimientos ortopédicos con
inserción de prótesis. (BIII).
-
Cirugía cardiológica con
esternotomías. (AI)
Histerectomías.(A1)
Cesáreas primarias y las que involucren
ruptura prematura de membranas.(A1)
b) La PAP es opcional
- Cirugías de mama y hernias, existen
variables que pueden aumentar el riesgo de infección
como es la duración > 2 horas, evaluación prequirúrgica con ASA de 3,4 o 5.(BI)
- Cirugías limpias con un riesgo
incrementado de
infección (BIII)
c) No existen datos evaluables para
"procedimientos mínimamente invasivos" como son las colecistectomías
laparoscópicas y para resecciones intestinales para ser recomendados de forma estándar
(BIII)
d) Los procedimientos urológicos abiertos
que involucren el intestino están inmersos dentro de las recomendaciones que se dan para
cirugía general (BIII) La literatura relacionada a procedimientos transuretrales es
controversial, sugiriéndose la esterilización de la orina previa a la manipulación.
e) Los procedimientos que involucre a
recién nacidos es común la práctica de utilizar antibióticos de amplio espectro como
PAP en muchos procedimientos que involucran a menores de 30 días, no existe datos
suficientes para justificar esta práctica.(CIII)
Principios en la administración de la
PAP
Dosis
Existen pocos trabajos relacionados a la
importancia de la dosis en la PAP, sin embargo se recomienda que la dosis utilizada nunca
puede ser menor a la dosis terapéutica estándar de la droga utilizada incluso dada la
corta duración y probada seguridad de los fármacos utilizados en la PAP, es razonable el
uso de dosis altas a las recomendadas para su uso terapéutico. Ej: cefazolina 1 a 2g.
Vía de administración
La administración endovenosa es el método
ideal para alcanzar niveles adecuados en los tejidos durante muchos procedimientos
quirúrgicos.12 Hay una excepción a este principio que es la cirugía
colorectal, como ya lo mencionamos anteriormente existen trabajos en donde sólo la
preparación del intestino con antibióticos por via oral parecería ser una alternativa
tan efectiva como la parenteral23 de la misma manera otros investigadores
sugieren la combinación de ambas vías.
Tiempo
La meta de la PAP es alcanzar niveles
antimicrobianos inhibitorios en la incisión quirúrgica y mantener niveles adecuados
durante todo el procedimiento quirúrgico. Los agentes utilizados parenteralmente podrían
ser administrados dentro de los 60 minutos previa a la incisión, aunque lo ideal sería
inmediatamente previo a la misma.9 En cesárea la administración de la PAP
debe de ser inmediatamente clampeado el cordón umbilical.
Duración
La duración óptima de la PAP no se
conoce. Muchos reportes han documentado efectividad con dosis única (BII), es probable
que no haya beneficios con dosis adicionales. Este principio está bien establecido para
cirugías de vía biliar, gástrica, colónica, histerectomía y prostatectomía
transuretral.12 Hasta que no exista una recomendación la administración de
dosis postoperatoria no está indicada ( CIII) o no debería continuarse luego de las 24
horas del procedimiento quirúrgico (BIII). Existen varios trabajos donde se compara
monodosis con dosis múltiples y en donde se comprobó que existe diferencias en la
frecuencia de infección de herida quirúrgica.24 La duración de la PAP en
cirugía cardiovascular está en debate y muchos investigadores sugieren prolongar la PAP
(CIII), sin embargo la continuación de la PAP hasta la remoción de todos los catéteres
y drenajes no es apropiada,9 de la misma manera existen trabajos donde no se ha
demostrado ningún beneficio el prolongar más de 48 horas la PAP, y se ha observado que
la monodosis es tan efectiva como esquemas de dosis múltiple en cirugía cardiovascular.25,26
La necesidad de administrar dosis
adicionales durante un procedimiento quirúrgico no está completamente definido, sin
embargo una serie de trabajos han documentado la disminución de la efectividad de la PAP
en procedimientos prolongados
y cuando los niveles de la droga en suero y
tejidos son bajos.27,28,29,30 Las recomendaciones al momento son la de
administrar dosis adicional de antimicrobiano cuando han transcurrido una o dos vidas
media de la droga elegida ó más de 3 horas de cirugía (C III).8,9
Implementación
La normatización de PAP debería ser
incorporada dentro de los procedimientos rutinarios realizados en el quirófano sea por
parte de los anestesiólogos o por la enfermera circulante. La dosis, vía, tipo de
antimicrobiano deben de ser revisados en relación a las indicaciones sugeridas por el
cirujano.
Para ayudar a la implementación de las
normas de PAP, deberían de conformarse los comités multidisciplinarios integrado por
cirujanos, infectólogos, anestesiólogos y enfermeras con la participación de personal
de quirófano, farmacia, y comité de control de infecciones, los cuales deben de elaborar
recomendaciones para la elección de las drogas a utilizar y los procedimientos de las
mismas. Existen varias guías que pueden servir de ayuda para la elaboración de las
mismas, una de la más utilizadas es la de la Sociedad Americana de Enfermedades
Infecciosas que puede ser adaptada o modificada a las necesidades de cada Institución.
Guía de Profilaxis Antibiótica en
Cirugía. 31,32
Dosis recomendadas en Pediatría:
1- Cirugía en Ortopedia y
Traumatología:
A- Colocación de prótesis articulares
y material de osteosíntesis:
Elección :Cefazolina 1 g. preinducción,
luego 1 g. c/ 8 horas x 24 horas
B- Fractura expuesta I, II, III a:
Elección :Cefazolina 1 g. preinducción,
luego 1 g. c/ 8 horas x 24 horas
C- Amputación:
Elección: Clindamicina 600 mg más
Gentamicina 1.5mg/kg mg preinducción, luego Clindamicina 600 mg c/ 8 horas más
gentamicina 3 mg/Kg monodosis diaria por 24 horas.
ia: inducción anestésica
2- Cirugía de cabeza y cuello:
A. Amigdalectomía/adenoidectomía: No
hay datos que sustenten una recomendación de profilaxis.
B. Cirugía rinológica con realización de
injerto, reoperación:
Elección:Cefazolina 2 g. en la
preinducción, como única dosis.
C. Cirugía que atraviesa cavidad oral o
cirugía mayor de cabeza y cuello:
Elección :Clindamicina 600 mg. más
Gentamicina 1.5mg/ Kg preinducción, luego
Clindamicina 600 mg. c/ 8 horas mas
gentamicina 3mg/Kg c/24 por 24 horas.
Elección : Cefazolina 1 g. preinducción:
única dosis
3- Cirugía plástica: Profilaxis:
Opcional
Elección : Cefazolina 1 g. preinducción:
única dosis
4- Cirugía oftalmológica:
No hay estudios adecuadamente
controlados que avalen estas recomendaciones (CIII)
A- Traumatismo penetrante:
Ciprofloxacina 750 mg cada 12 horas vía
oral por 24 horas
Excepciones :
1. Si el traumatismo tiene factores de
riesgo para infección por B.cereus: objeto de metal, madera ó en áreas rurales:
Agregar Clindamicina 600 mg cada 8 horas por 24 horas.
2. Si se usa vía Ciprofloxacina endovenosa
(EV) 200 mg cada 12 horas.
B. Cirugías oftalmológicas programadas
(todas las otras)
Administración tópica de Gentamicina o
Tobramicina en gotas desde la noche previa.
Al finalizar la cirugía: administración
subconjuntival de Cefazolina ó Cefalotina 100mg.
Profilaxis antibiótica sistémica:
Cefazolina ó Cefalotina 1g. preinducción u Ofloxacina 400 mg vo.
5 - Cirugía torácica:
A- Resección pulmonar, cirugía de
mediastino:
Elección: Cefazolina 1 g. preinducción,
luego 1 g. cada 8 horas por 24 horas
Nota: No requieren profilaxis
antibiótica (ATB) la colocación de tubo pleural y el traumatismo de tórax.
En el traumatismo de tórax que requiere
colocación de tubo pleural, 24 horas de profilaxis ATB con cefalosporinas de 1era podría
ser de utilidad.
6- Cirugía vascular:
A- Colocación de prótesis vasculares
(centrales ó periféricas):
Elección : Cefazolina 1 g. preinducción,
luego 1 g. c / 8 horas por 24 horas
B- Colocación de marcapaso definitivo:
Elección : Cefazolina 1 g. preinducción,
como única dosis.
C- Otra cirugía vascular sin colocación
de prótesis arteriales:
Elección: Cefazolina 1 g. preinducción,
luego 1 g. c / 8 horas por 24 horas
No requieren profilaxis : Colocación de
Swang- Ganz, colocación de marcapasos transitorios, estudios hemodinámicos y
arteriografías.
No indicada: Cirugía de várices y, salvo
que la cirugía dure más de 4 horas en que debe extenderse a 24 horas.
D- Cirugía cardiovascular central con ó
sin colocación de material protésico
Elección: Cefazolina 1 g. preinducción,
luego 1 g. cada 8 horas por 24 horas.
RVM- Revascularización Miocárdica.
7- Neurocirugía:
A. Craneotomía (incluye exploración
con endoscopio) y otras cirugías limpias de cráneo que no atraviesan mucosa sinusal u
oral. Laminectomía:
Elección: Cefazolina 1 g. preinducción,
como única dosis.
B. Cirugía transesfenoidal y otras
cirugías que atraviesan mucosas sinusal u oral :
Elección: Clindamicina 600 mg
preinducción, luego 600 mg cada 8 horas por 24 horas.
C. Colocación de sistemas de derivación
de LCR:
Elección : Ceftriaxone (CRO) l g IV
8- Cirugía urológica:
Nota : Las recomendaciones para
cirugía urológica se consideraron separadamente en la evaluación realizada por el IDSA,
la heterogeneidad de trabajos y resultados constituye una dificultad para calificarlas. Se
clasificaron como C III.
Consideraciones Básicas:
Previo a realizar cualquier
procedimiento urológico quirúrgico o endoscópico, debe realizarse urocultivo.
No se recomienda utilizar antibióticos en
los pacientes con sonda vesical, asintomáticos.
Cirugía urológica que no involucra
vísceras del tubo digestivo (endoprostática, endovesical, abdominal o nefrectomía).
Urocultivo negativo:
Elección : Cefazolina 1 g.
preinducción, como única dosis.
Urocultivo positivo:
Si fuera posible, deberá completar
tratamiento antibiótico (duración 7 a 10 días), y certificar negativización del
urocultivo de control previo al procedimiento.
Si no puede postergarse la cirugía deberá
iniciarse ATB adecuado al cultivo, realizando el procedimiento luego de las 72 horas, con
una dosis de ATB preinducción.
B- Cirugía urológica abdominal que
involucra vísceras del tubo digestivo :
Elección : Metronidazol 500 mg. EV más
Gentamicina 1.5mg /Kg EV preinducción.
Realizar previamente la misma preparación
que para cirugía colorrectal.
Elección : Cefazolina 1 g. preinducción,
como única dosis.
9- Cirugía esófago-gastro-duodenal:
Elección: Cefazolina 1 g.
preinducción, como única dosis.
A- Cirugía colorrectal e intestino
delgado:
Si bien la literatura avala la
Preparación Mecánica + ATB orales como alternativa a los ATB endovenosos en cirugía
colónica y de intestino delgado, se recomienda Preparación mecánica + Profilaxis ATB
EV, teniendo en cuenta la frecuente práctica de utilizar ambos sistemas simultáneamente
y el aumento de costos que ello conlleva.
a) Preparación mecánica del colon: se
realizará la mańana previa a la cirugía con polietilenglicol 4 litros, que serán
ingeridos en 3 horas. Pueden utilizarse otros sistemas alternativos de limpieza mecánica
de colon.
b) Profilaxis Antibiótica:
Elección: Metronidazol 500 mg ú ornidazol
1 g. EV más Gentamicina 1.5 mg/Kg preinducción, como única dosis.
B- Apendicectomía:
Elección: Metronidazol 500 mg ú
Ornidazol 1 g. EV más Gentamicina 1.5 mg/ Kg. Preinducción única dosis.
En caso de comprobar perforación o
gangrena se continuará por 3- 5 días los mismos ATB.
C- Traumatismo penetrante de abdomen:
Elección: Metronidazol 500 mg ú
Ornidazol 1 g. EV más Gentamicina 1.5 mg / Kg preinducción.
En caso de comprobar perforación de
víscera hueca se continuarán los mismos ATB por 3 a 5 días.
10- Cirugía ginecológica y obstétrica:
A- Histerectomía abdominal o
vaginal y cirugía vaginal:
Elección: Cefazolina 1 g.
preinducción, como única dosis.
B- Aborto:
B1) Espontáneo 1er trimestre:
Doxiciclina 200 mg. Por vía oral y luego 100 mg cada 12 horas por 24 horas (en especial
si Factores de Riesgo - FR- para Enfermedades de Transmisión Sexual (ETS) ó antecedentes
de Enfermedad Pelviana Inflamatoria (EPI).Alergia a Tetraciclinas: Clindamicina 600 mg
más Gentamicina 1.5 mg/Kg preinducción.
Nota: Realizar tratamiento completo si se
documenta C. trachomatis y/o N. gonorrhoeae en estudios previos al procedimiento
B2) Primer trimestre con sospecha de
maniobras abortivas, Segundo y Tercer trimestre:
Elección: Cefazolina 1 g. preinducción,
luego 1 g. cada 8 horas por 24 horas.
C- Cirugía mamaria:
Elección: Cefazolina 1 g.
preinducción, como única dosis.
D- Colocación de DIU e
histerosalpingografía:
Doxiciclina 200 mg por vía oral 2
horas antes del procedimiento.
Alergia a Tetraciclinas: Clindamicina 600
mg VO 2 horas antes del procedimiento.
E- Cesárea:
Elección: Cefazolina 2 g.
inmediatamente luego de clampear el cordón como única dosis.
11.Procedimientos mínimamente invasivos :
Se utilizarán los esquemas propuestos
para los procedimientos convencionales correspondientes.
12. Profilaxis antibiótica en
mordeduras humanas y animales:
El inicio de la profilaxis antibiótica
de las mordeduras debe comenzar dentro de las primeras 24 horas luego de la injuria,
preferiblemente dentro de las 8 horas.
Simultáneamente debe realizarse limpieza
agresiva y debridamiento quirúrgico si fuera necesario.
Esquema de elección: Amoxicilina / Ac.
Clavulánico 500mg cada 8 horas v.o. por 3 a 5 días.
Bibliografía
1. Cruse P. History of surgical
infection. En Fry DE, Surgical infections. 1a ed. Boston, Little Brown and
Company;1995:3-9.
2. Kernodle DS, Kaiser AB. Postoperative
infections and antimicrobial prophylaxis. En Mandell GL, Bennett JE, Dolin R., eds,
Mandell, Douglas and Bennett's Principles and Practice of Infectious Disease, 4ta. New
York, Churchill Livingstone,1995: 2742-55.
3. Kluytmans J. Surgical Infections
Including Burns. En Wenzell RP, Prevention and Control of
Nosocomial Infections, Baltimore,
Williams & Wilkins, 1997: 841-64.
4. Ulualp K, Condon RE. Antibiotic
Pprophylaxis For scheduled operative procedures. En Dellinger PE (ed): Surgical
Infections. Infect Dis Clin North Am 1992: 3:613-625
5. Jensen W . Profilaxis Antimicrobiana
en Cirugia. Rev Chil Infect 2000; 17 ( Supl.1): 8 - 12
6. Novelli A. Antimicrobial prophylaxis
in surgery: The role of pharmacokinetics. J Chemother 1999;6:565 - 72.
7. Trilla A, Mensa J. Preoperative
Antibiotic Prophylaxis. En Wenzell RP, Prevention and Control of Nosocomial Infections,
Baltimore, Williams & Wilkins, 1997: 866-87.
8. Meakins JL. Guidelines for Prevention
of Surgical Site Infection. En Meakins SL. Surgical Infections Diagnosis and Treatment.
Scientific American, Inc., New York 1994:139-149.
9. Dellinger EP, Gross PA, Barrett TL,
Krause PJ, Martone WJ, McGowan JE, Sweet RL , Wenzel RP. Quality standard for
antimicrobial prophylaxis in surgical procedures. Clin Infect Dis 1994;18:422-7.
10. Smyth ET, Emmerson AM. Surgical site
infection surveillance. J Hosp Infect 2000;45:173-84
11. Mangram A, Horan TC, Pearson M,
Silver LC, Jarvis WR. Guideline for prevention of surgical site infection. Infect Control
Hosp Epidemiol 1999; 20:247 - 277.
12. Waddell TK, Rotstein OD.
Antimicrobial Prophylaxis in Surgery. Can Med Assoc J 1994; 151: 925 - 931.
13. Giuliani B, Periti E, Mecacci F.
Antimicrobial Prophylaxis in Obstetric and Gynecological Surgery. J Chemother 1999;11:
577-580
14. Mahmood A. Bacteriology of surgical
site infections and antibiotic susceptibility pattern of the isolates at a tertiary care
hospital in Karachi. JPMA J Pak Med Assoc 2000;50:256-9.
15. Vilar-Compte D; Mohar A; Sandoval S;
de la Rosa M Gordillo P; Volkow P Surgical site infections at the National Cancer
Institute in Mexico: a case-control study. Am J Infect Control 2000;28:14-20
16. Vermillion ST; Lamoutte C; Soper DE;
Verdeja A. Wound infection after cesarean: effect of subcutaneous tissue thickness. Obstet
Gynecol 2000;95 (6 Pt):923
17. Niessen M, Voss A. Incidence of
surgical site infections in pediatric patients: a 3-month prospective study in an academic
pediatric surgical unit. Pediatr Surg Int 2000;16:417-20
18. Kalmeijer MD, van Nieuwland-Bollen E
Bogaers-Hofman D, de Baere GA Nasal carriage of Staphylococcus aureus is a major risk
factor for surgical-site infections in orthopedic surgery. Infect Control Hosp Epidemiol
2000;21:319-23
19. Kirton OC, O'Neill PA, Kestner M,
Tortella BJ. Perioperative antibiotic use in high-risk penetrating hollow viscus injury: a
prospective randomized, double-blind,placebo-control trial of 24 hours versus 5 days J
Trauma 2000;49:822-32
20. Smyth ET, Emmerson AM. Surgical site
infection surveillance. J Hosp Infect 2000 ;45:173-84
21. Norden C, Gillespie WJ, Nade S.
Infections in Bones and Joints. Antimicrobial agents and other forms of therapy used in
the treatment on bone infections. Blackwell Scientific Publications, Boston 1994, 119 -134
22. Dellinger EP, Gross PA, Barrett TL,
Krause PJ, Martone WJ, McGowan JE, Sweet RL , Wenzel RP. Quality Standard for
Antimicrobial Prophylaxis in Surgical Procedures. The Infectious Disease Society of
America. Infect Control Hosp Epidemiol 1994;15(3): 182-8
23. Nichols RL. Efficacy of preoperative
antimicrobial preparation of the bowel. Ann Surg 1972; 172 :227-2.
24. Stone HH, Haney BB, Kolb LD, Geheber
CE, Hooper CA. Prophylactic and preventive antibiotic therapy, timing, duration and
economics. Ann Surg. 1979;186: 691-9.
25. Harbarth S, Samore MH, Lichtenberg
D, Carmeli Y. Prolonged antibiotic prophylaxis after cardiovascular surgery and its effect
on surgical site infections and antimicrobial resistance. Circulation 2000; 27:
101:2916-21.
26. Bucknell SJ. Single vs Multiple dose
antibiotics prophylaxis for cardiac surgery. Aust NZ J Surg. 2000; 70: 409-11.
27. Shapiro M, Munoz A, Tager IB,
Schoenbaum SC, Polk BF. Risks factors for infection at the operative site after abdominal
or vaginal hysterectomy. N Engl J Med 1982; 307: 1661-6
28. Kaiser AB, Heerington JL Jr, Jacobs
JK, Mulherin JL Jr et al. Cefoxitin vs erythromicin, neomycin and cefazolin in colorectal
operations. Importance of the duration of the surgical procedure. Ann Surg 1983; 198:
525-30
29. Golman H. Cephalothin prophylaxis in
cardiac valve surgery: a prospective double-blind comparison of two-day and six-day
regimen. J Thorac Cardiovasc Surg. 1997: 73:470-9
30. Platt R. Antibiotic prophylaxis for
cardiovascular surgery: Efficacy with coronary artery bypass. Ann Intrn Med. 1984: 101;770
- 4
31. Hospital Italiano de Buenos
Aires,Revista. Programa para la racionalizacion del uso de antimicrobianos hospitalarios,
1995
32. Calmaggi A, Gonzalez M, Inchauspe A,
Clara L, Defelitto J., Profilaxis antibiótica en Cirugía, Sociedad Argentina de
Infectología (SADI) 1996.
|